
脑机接口被认为是下一代智能医疗与人机交互的重要方向。当前主流脑机接口大多建立在电磁学框架之上,但电刺激与电磁传输在深部组织穿透、实时反馈以及无线化方面始终面临挑战。相比之下,超声作为一种机械波,兼具深组织穿透、高空间分辨率以及与脑电/心电兼容等优势,因此近年来逐渐被认为是构建新一代脑机接口(即Ultrasonic Brain–Machine Interface, uBMI)的重要候选技术。特别是在超声神经调控、无线供能以及生理反馈等方向,超声展现出了巨大的发展潜力。
然而,真正实现超声脑机接口仍面临几个关键瓶颈。首先,颅骨和肋骨等复杂生物屏障会对超声产生强烈散射和相位畸变,使超声波形严重失真;其次,大脑与心脏等复杂生理系统往往需要多靶点协同调控,而传统超声方法难以实现精准稳定的多焦点控制;此外,闭环脑机接口还需要根据实时生理状态动态调节刺激,同时实现稳定的无线供能与信息通信。
针对这些问题,复旦大学智慧医疗超声课题组提出了一种基于声学超表面的集成超声调控平台,实现了复杂生物屏障后的精准超声调控、实时生理反馈闭环控制,以及同步无线供能与数据通信(图1)。相关成果以 “Integrated Ultrasonic Platform for Bioelectronic Control Through Biological Barriers Based on Metasurface” 为题发表在 Advanced Science。该研究由复旦大学智慧医疗超声课题组完成,第一作者为博士生张传鑫,通讯作者为江雪教授和他得安教授。
从相位补偿走向物理约束波动设计
传统超声超表面设计通常基于相位全息原理,即先计算目标声场,再通过局域相位匹配实现波前调控。然而,这类方法通常建立在局域近似基础之上,难以准确描述复杂生物环境中的真实波动行为。当超声穿过颅骨或肋骨时,内部会同时出现多重散射、结构衍射、剪切波转换以及基元间非局域耦合等复杂过程,导致传统设计方法在复杂介质中迅速失效。
针对这一问题,研究团队提出了一种“融合全波物理约束(PCGS)的人工智能设计”方法。研究不再将颅骨/肋骨等生物屏障简化为均匀介质或仅进行相位-厚度补偿,而是基于CT数据重建包含真实几何形貌与非均匀声学属性的三维模型,并将超声在超表面、骨组织及软组织中的传播过程整体纳入优化框架。团队进一步建立了耦合角谱-有限元模型,在保持计算效率的同时,实现了复杂介质中的高精度全波传播计算。
这一方法本质上实现了从“经验相位补偿”向“物理约束逆向设计”的转变。实验结果表明,在穿过颅骨后,该方法仍能够实现稳定的多焦点超声聚焦,多焦点强度误差由传统方法的±33% 降低至±6.5%,显著提升了复杂环境中的聚焦精度与稳定性(图2)。这一结果表明,超声超表面正从被动波前修正器演变为适应复杂生物环境的主动声学界面,也说明复杂非均质介质中的声波精准调控开始具备面向真实生物环境的可行性。
让超声“理解”生理状态:从开放刺激走向闭环调控
在实现精准声场控制后,研究团队进一步探索了超声与实时生理反馈结合的可能性。
研究团队构建了一套基于脑电(EEG)的注意力闭环超声系统。系统能够实时监测人的注意力状态,当检测到注意力下降时,自动调节超声刺激强度,并通过超表面实现穿颅精准能量无线传输。这意味着超声刺激不再是固定输出,而开始具备依据实时脑状态动态变化的能力,从而形成感知—反馈—调控的闭环机制。这一结果的重要意义在于,它将实时脑状态反馈直接耦合进超声调控链路,为未来超声脑机接口中的自适应神经调控提供了新的技术框架。相比传统电刺激系统容易受到刺激伪影干扰,超声与EEG之间天然的低干扰特性,使其在闭环神经调控中具备独特优势。
除脑调控外,研究团队进一步将这一框架扩展至心脏场景。由于肋骨会对超声产生类似“衍射光栅”的效应,传统聚焦方法容易形成多重衍射旁瓣,导致焦点扩散和能量泄漏。研究团队利用PCGS超表面显著抑制了这些旁瓣,并实现了与心跳周期同步的超声刺激。这意味着超声不仅能够实现空间上的精准定位,还能够在时间维度与生理节律实现同步,为未来无创超声起搏、心律调控以及心脏闭环治疗提供了新的可能。
超声不仅传能量,还能传信息
对于未来植入式脑机接口而言,仅有刺激功能远远不够。系统还需要长期稳定的无线供能与数据通信能力。为此,研究团队提出了一种双频超声通信架构,以同一个超表面器件同时调控双频率超声,其中500 kHz超声波用于无线供能,600 kHz超声波用于数据通信,两种频率通过同一个超表面和同一声学通道同时传输,实现了“能量+信息”的同步超声传递。实验中,即使供能信号与通信信号之间存在高达400倍的功率差异,系统仍能够稳定恢复脉搏波形、心率间隔(IBI)以及 BPM 等生理数据。这一结果说明,超声不仅能够传递能量,还能够同时承担信息编码、通信与反馈调控等功能,为未来超声脑机接口中的无线化、微型化植入器件提供了新的物理实现路径。
面向未来超声脑机接口的新物理框架
这项研究的意义并不仅仅在于实现了几个独立功能,更重要的是,它将精准波前控制、实时生理反馈、无线供能与通信等重要需求统一到同一个超声物理平台之中。相比传统脑机接口主要依赖电子学与电磁学框架,本研究说明复杂生物环境中的机械波调控也可能成为未来脑机接口的重要物理基础。这种统一波前控制、反馈调控与无线运行的超声框架,为未来超声脑机接口的发展提供了一条新的技术路线。
未来,结合可重构超表面、人工智能优化以及微型植入器件,超声脑机接口有望进一步发展成为一种能够“感知—决策—调控”一体化运行的新型生物电子系统,在神经疾病治疗、脑功能调控、无创心脏治疗等方向展现广阔应用前景。
该研究得到国家重点研发计划、国家自然科学基金、上海市曙光计划、上海市基础研究特区、上海启源青年学者、小米青年学者等项目支持。
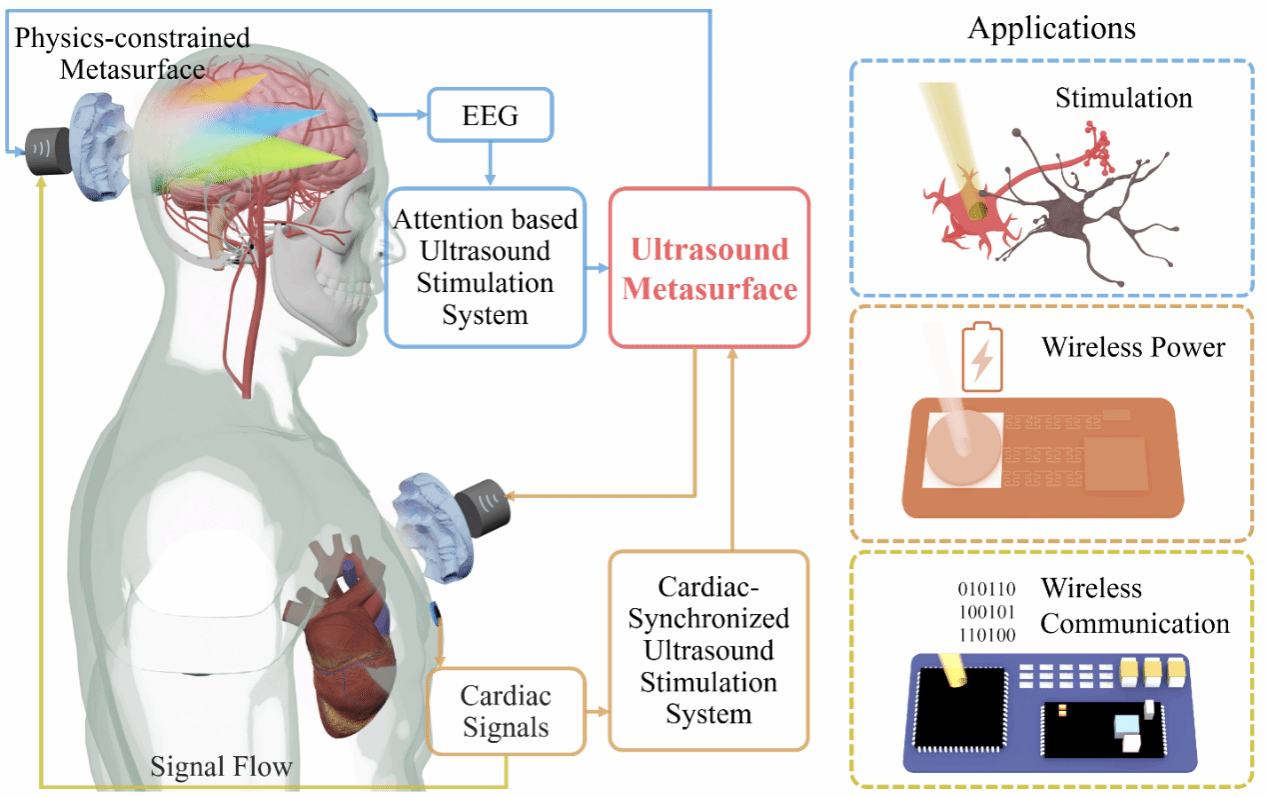
图1:面向超声脑机接口的集成超声平台总体框架。构建了一种基于声学超表面的集成超声平台,将复杂生物屏障后的超声波前调控、实时脑电/心电反馈以及无线供能与数据通信统一到同一个物理框架中。超声因此不再只是单纯的刺激工具,而开始同时承担能量传输、生理反馈以及无线通信等功能。这种“波前控制—生理反馈—无线运行”一体化架构,为未来超声脑机接口(uBMI)和闭环生物电子系统提供了新的总体设计思路。
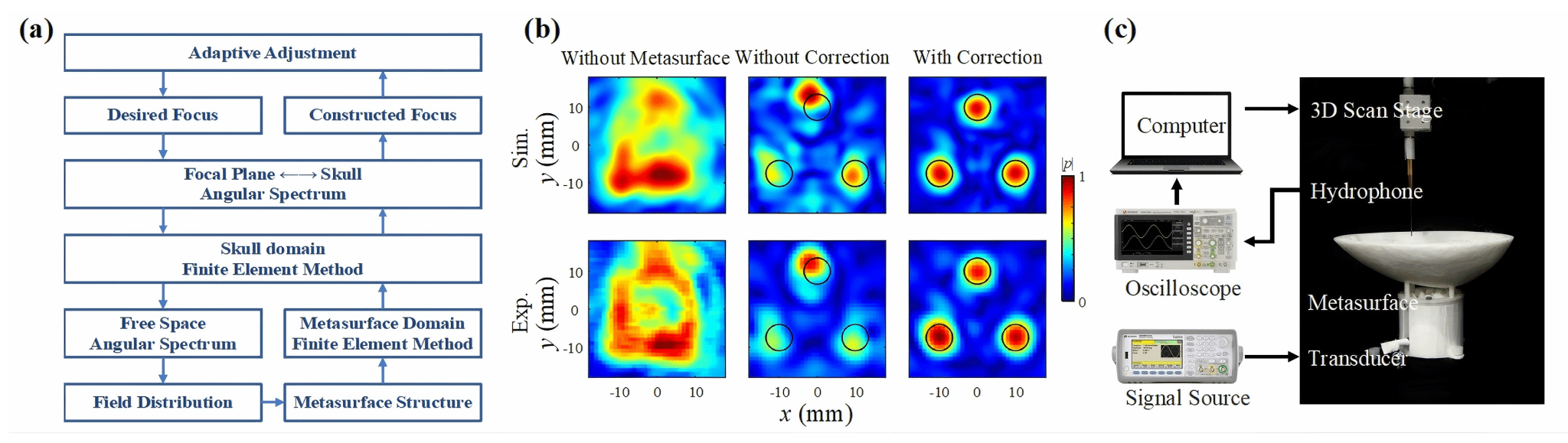
图2:PCGS物理约束超表面设计原理与穿颅多焦点控制。融合全波物理约束的PCGS超表面设计方法,将超声在超表面结构、颅骨以及软组织中的传播过程统一纳入优化链路,实现了复杂生物环境中的高精度波前控制。在穿颅实验中,经过PCGS校正后,多焦点超声场在穿过颅骨后仍维持稳定聚焦,而未经校正时焦点则明显偏移与畸变。这意味着超声脑机接口中的深脑精准调控具备了面向复杂真实生物环境的高保真波场基础。
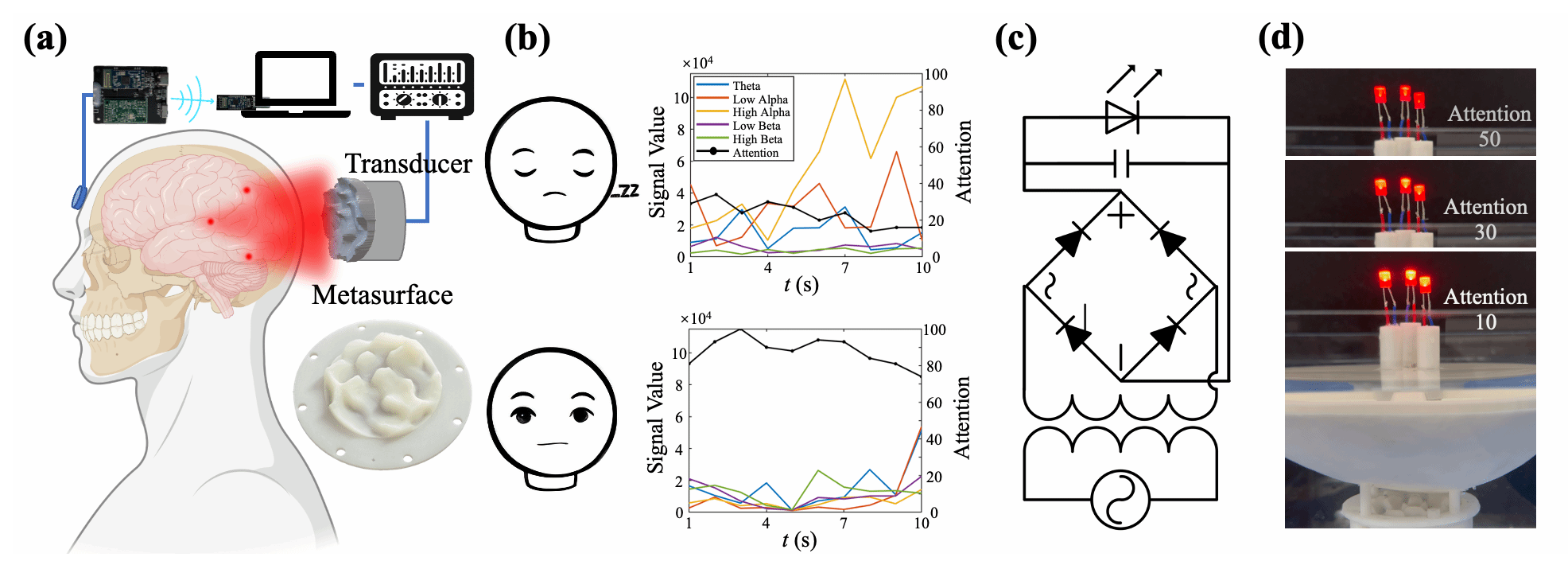
图3:基于脑状态反馈的闭环穿颅超声调控。EEG反馈被直接耦合进超声调控链路,使超声刺激开始具备依据实时脑状态动态变化的能力。系统实时解析注意力水平,并在注意力下降时自动调节穿颅超声输出,同时通过超表面实现精准能量传输。不同认知状态下,脑电频谱与注意力指标呈现显著差异,而超声输出则随脑状态动态变化,为未来超声脑机接口中的自适应神经调控提供了新的物理框架。
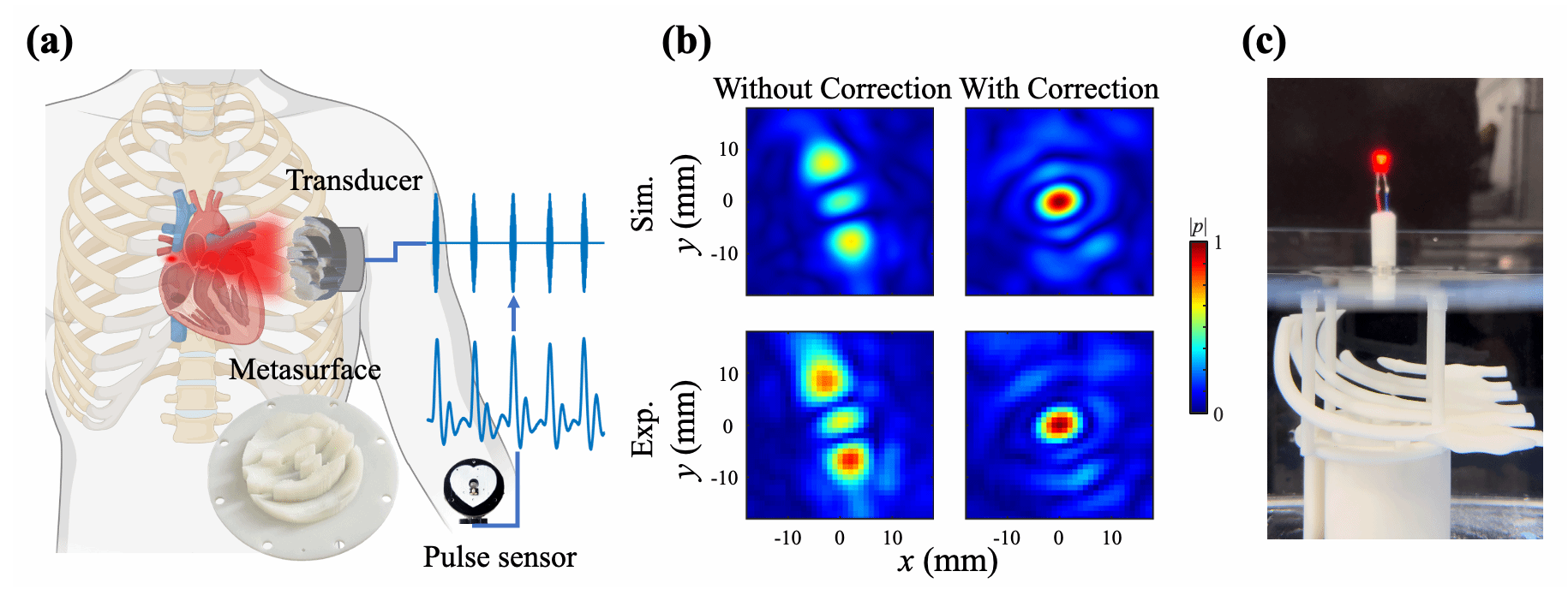
图4:穿肋骨同步超声刺激实现时空协同调控。由于肋骨会对超声产生强烈衍射效应,传统聚焦方法容易形成多重副焦点并导致能量泄漏。PCGS超表面通过预补偿波前,有效抑制了肋骨引起的衍射旁瓣,并恢复了稳定的主焦点。同时,实时脉搏信号被用于同步调制超声输出,使刺激过程能够与心跳周期精确对齐。超声因此不仅能够在空间上实现精准聚焦,还开始具备与生理节律动态同步的能力,为未来自主闭环调控、无创心脏刺激以及智能生理干预提供了新的技术基础。
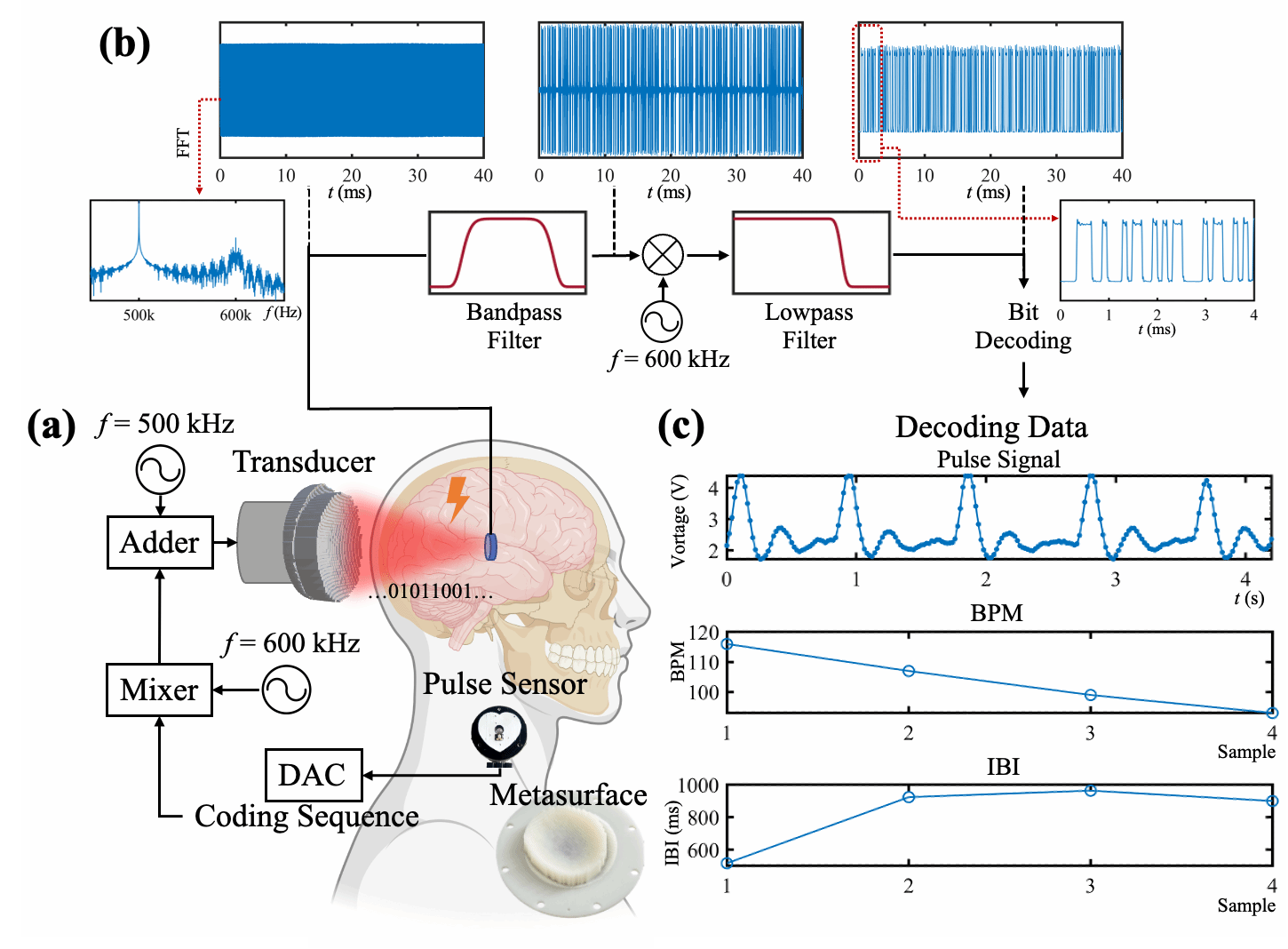
图5:超声无线供能与数据通信一体化系统。针对未来植入式脑机接口对无线化运行的需求,提出了一种双频超声通信架构,通过同一个超表面和同一声学通道同步实现无线供能与数据通信。其中500 kHz超声用于能量传输,600 kHz超声用于数据通信,即使两者之间存在高达400倍的功率差异,系统仍能够稳定恢复脉搏波形、IBI以及BPM等生理信息。整个过程中,超声不仅承担能量输运功能,还实现了信息编码、传输与解调。